ผมไม่แน่ใจว่าจะมีใครบ้างมั้ยที่เคยชมภาพยนตร์สั้น "นับหนึ่งถึงชั้น11" เรื่องราวของหมอนักวิจัยคิดค้นยารักษาโรคไข้เลือดออกที่ต้องต่อสู้กับทั้งปัญหาในการวิจัยที่ยากจนดูไม่มีความหวังและทำให้คนในทีมท้อและขอออกจากทีมวิจัย และยังต้องต่อสู้กับปัญหาครอบครัวที่เหมือนแฟนสาวจะไม่เข้าใจในสิ่งที่เขาทำผมกำลังจะบอกว่าภาพยนตร์สั้นเรื่องนี้ค่อนข้างที่จะสื่อความรู้สึกของนักวิจัยฯได้ดีในระดับหนึ่งเลย ความรู้สึกกดดันที่ต้องรับมือกับปัญหาในการทำวิจัยและปัญหาครอบครัว
ผมในฐานะของนักศึกษาคณะเภสัชฯที่ตอนนี้กำลังศึกษาและสนใจงานทางด้านวิจัยและพัฒนายาอาจจะยังมีประสบการณ์น้อย แต่วันนี้ก็อยากแชร์เรื่องราวของการที่กว่าจะมาเป็นยาให้ทุกคนได้ใช้กันในปัจจุบัน นักวิจัยต้องดิ้นรนกันขนาดไหนเพื่อให้ได้มาซึ่งยาที่มีประสิทธิภาพ มีคุณภาพ และที่สำคัญมีความปลอดภัยต่อการนำไปใช้
หากผิดพลาดประการใดต้องขออภัยมา ณ ที่นี้ ด้วยนะครับ
ในตอนนี้ผมจะให้ทุกท่านสมมติตัวเองว่า เราเป็นนักวิจัยต้องการทำยาแก้ปวดขึ้นมาสักตัวหนึ่งเราจะต้องทำอย่างไรบ้าง ?
เพื่อให้เข้าใจง่ายมากขึ้นผมจะขอแบ่งช่วงระยะเวลาในการเดินทางของยาออกเป็นช่วงๆ เป็น 4 ช่วงนะครับ
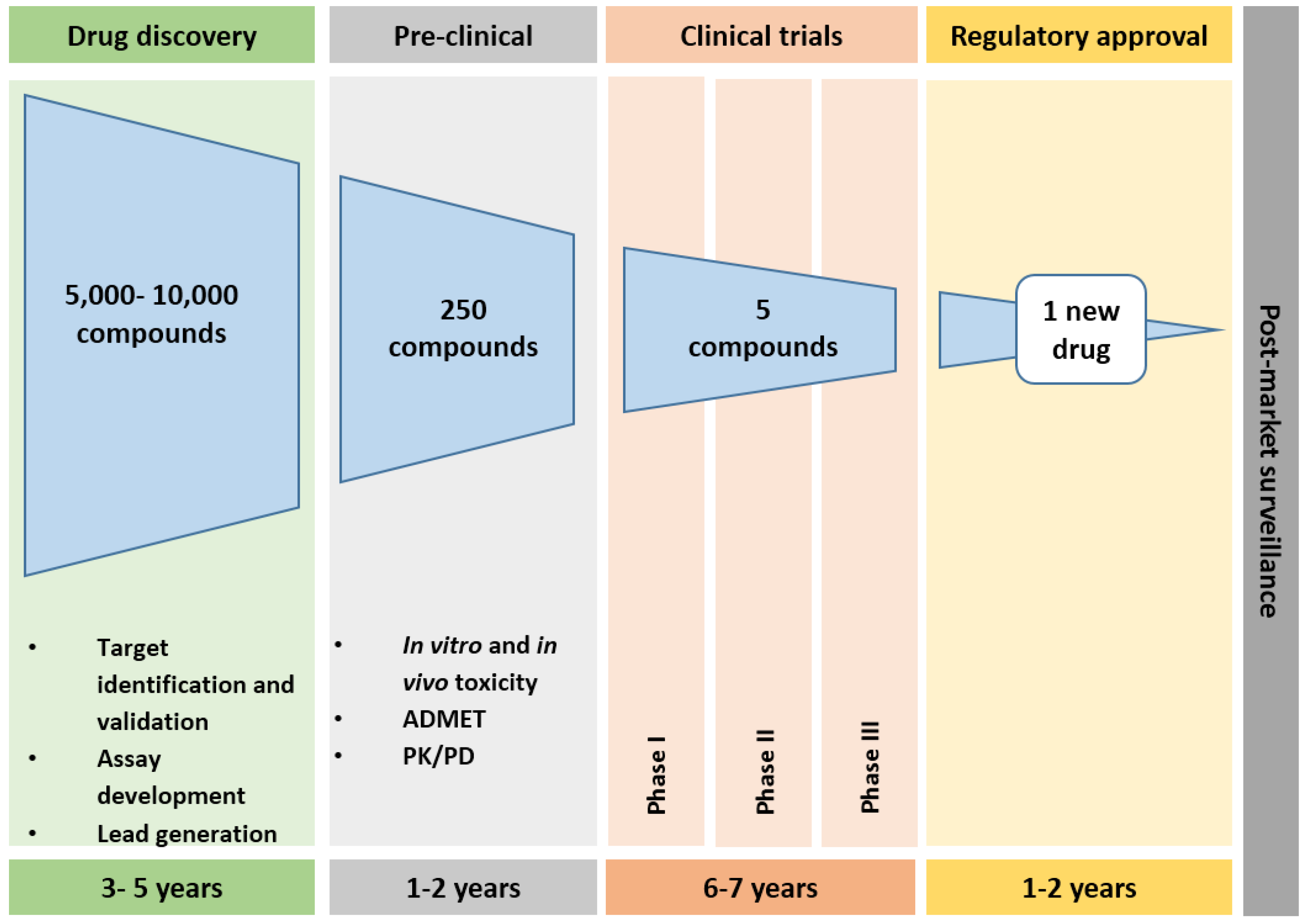 ภาพแสดงแต่ละช่วงเวลาในการเดินทางของยา แหล่งที่มา : http://stehlin.org
1. Drug discovery
ภาพแสดงแต่ละช่วงเวลาในการเดินทางของยา แหล่งที่มา : http://stehlin.org
1. Drug discovery : เป็นขั้นตอนแรกสุดที่ใช้เวลาค่อนข้างยาวนาน หากเราจะวิจัยทำยาแก้ปวด เราจะต้องหาโครงสร้างโมเลกุลที่มีฤทธิ์ในการแก้ปวดให้ได้ก่อน ผมจะขอเรียกว่า
Lead compound นะครับ ซึ่งการที่จะให้ได้มาซึ่ง Lead compound เราสามารถทำได้โดยเช่น
- เราอาจเอาข้อมูลความรู้ที่มีการสั่งสมมาอย่างยาวนานว่าสมุนไพรใดที่สามารถแก้ปวดได้ เช่น บรรพบุรุษเราเคยใช้ต้น Willow (ไม่ใช่ Willow ในป่า payon นะครับ) ในการแก้ปวดและอักเสบได้ ดังนั้นเราก็ลองหาดูซิว่าใน Willow มันมีสารใดบ้างที่ออกฤทธิ์แก้ปวดได้บ้างเราก็สกัดออกมาจะได้สารผสม (crude extract) ซึ่งอาจมีโมเลกุลที่สามารถแก้ปวดได้หลายร้อยตัว (เว่อร์ไป 5555)
- ถ้าแอดวานซ์ขึ้นมาเราอาจต้องไปไล่ดูผลงานศึกษาวิจัยต่างๆว่าโครงสร้างใดบ้างที่ออกฤทธิ์แก้ปวดได้บ้าง เราก็รวบรวมข้อมูลมาให้มากที่สุด
ในขั้นตอนนี้จะเห็นได้ว่าการที่เราต้องหา Lead compound ที่มีฤทธิ์แก้ปวดนั้น จะทำให้เราได้โครงสร้างทางเคมีมา
เป็นหมื่นเป็นพันโครงสร้าง!!!
สาเหตุที่มีเยอะขนาดนั้นเป็นเพราะว่า โมเลกุลเหล่านั้นมีโครงสร้างส่วนหนึ่งที่สามารถออกฤทธิ์แก้ปวดได้เหมือนกัน โครงสร้างของโมเลกุลเหล่านั้น เราเรียกว่า
Pharmacophore ครับ
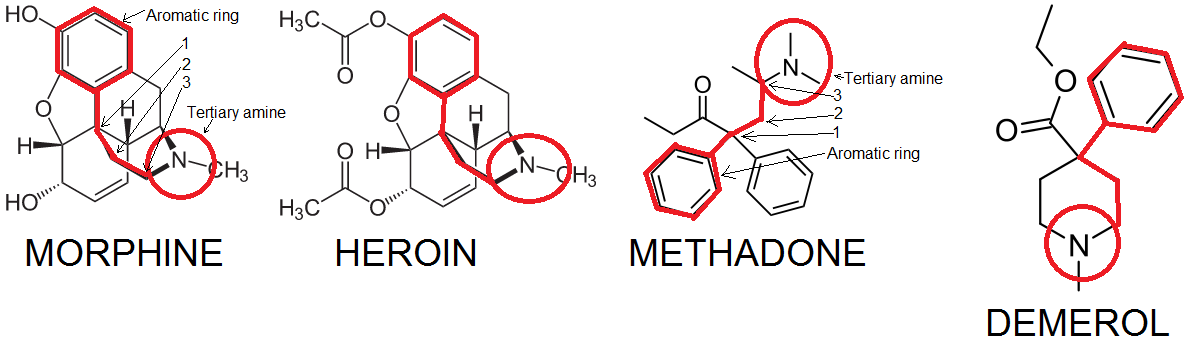 ภาพแสดงตัวอย่าง Pharmacophore ของโมเลกุลที่แตกต่างกันแต่จะมีโครงสร้างบางส่วนที่เหมือนกันในการออกฤทธิ์
ภาพแสดงตัวอย่าง Pharmacophore ของโมเลกุลที่แตกต่างกันแต่จะมีโครงสร้างบางส่วนที่เหมือนกันในการออกฤทธิ์
เท่ากับตอนนี้เราโครงสร้างอยู่ในมือเป็นหมื่นเป็นพันโครงสร้าง เราจะต้องคัดเลือกเพื่อหาโครงสร้างที่สามารถออกฤทธิ์ได้ดีที่สุด มีประสิทธิภาพที่สุด ปลอดภัยและเหมาะสมในการเอามาศึกษาพัฒนาต่อ ก็จะเข้าสู่ช่วงที่ 2
2. Pre clinical : ศึกษาคัดเลือกจากหลายพันโมเลกุล การคัดเลือกโดยธรรมชาติ ?
ซึ่งก็ใช้เวลาในการศึกษาที่ค่อนข้างนานเพราะเราอาจจะต้องศึกษาฤทธิ์ของแต่ละโมเลกุลๆไปเรื่อยๆเพื่อคัดเลือกให้ได้มาซึ่ง pharmacophore การศึกษาฤทธิ์ก็อาจใช้วิธีการต่างๆในห้องแลป หรือปัจจุบันสะดวกขึ้นมากก็จะใช้คอมพิวเตอร์ในการทำนายการออกฤทธิ์ ซึ่งโปรแกรมที่ใช้เช่น Autodock เป็นต้น ก็จะทำให้การคัดเลือกโมเลกุลสามารถทำได้ง่ายมากยิ่งขึ้น แต่การใช้คอมพิวเตอร์ในการทำนายการออกฤทธิ์ก็ยังไม่สามารถตอบคำถามได้ 100 % นะครับว่าโมเลกุลของเรามันดีจริง อย่างไรก็ต้องทำการศึกษาต่อในแลปอยู่ดี แต่การใช้คอมฯนั้นก็จะสามารถช่วยตัดคัดกรองโมเลกุลอื่นๆได้เยอะมากเลยทีเดียว ทำให้จากการที่เราต้องมานั่งสังเคราะห์โมเลกุลเพื่อเอาไปศึกษาผลในแลปเป็นหมื่นโมเลกุล(เหนื่อยตายก่อน)ก็อาจถูกตัดทอนเหลือไม่ถึงพันโมเลกุล
การทดลองในขั้น Pre clinical นี้จะต้องทำการศึกษาหลายขั้น ผมขอแบ่งง่ายๆเป็น
 ภาพแสดง in vitro study, in vivo study แหล่งที่มา : http://invivotransfection.com
ภาพแสดง in vitro study, in vivo study แหล่งที่มา : http://invivotransfection.com
-
in vitro study คือการทำการศึกษาประสิทธิภาพในการออกฤทธิ์ในเครื่องมือเครื่องแก้ว เช่นการทดลอง dpph assay ขั้นนี้จะไม่ใช้สัตว์ทดลองครับ
-
in situ study คือการทำการศึกษาประสิทธิภาพในเฉพาะอวัยวะนั้นๆ เช่นการศึกษาการยึดเกาะของยาบริเวณลำไส้ หรือการทดลองการคงอยู่ของยาในดวงตากระต่าย ขั้นนี้มีการใช้สัตว์ทดลองครับ หรือบางทีอาจใช้แค่บางส่วนครับ
-
in vivo study คือการทำการศึกษาในสัตว์ทดลองเลยครับ แน่นอนว่าหลังการทดลองกับสัตว์ทดลองแล้วเราต้องฆ่าสัตว์ทดลองด้วยวิธีการที่ไม่ทำให้เขาเจ็บปวดครับ T^T
ผลการศึกษาทั้งหมดจะทำให้เราทราบได้อย่างคร่าวๆว่า โมเลกุลที่เรามีอยู่เป็นร้อยนั้น แต่ละตัวมีประสิทธิภาพในการออกฤทธิ์อย่างไร มีความเป็นพิษต่อสัตว์ทดลองมั้ย (Toxicity) ถ้ามีก็ตัดทิ้ง ทำให้เรารู้ข้อมูลทางด้าน pharmacokinetics, pharmacodynamics อย่างคร่าวๆ เพื่อช่วยให้เราคัดเลือกโมเลกุลที่จะผ่านเข้ารอบต่อไปได้ง่ายขึ้นครับ
- pharmacokinetics คือ "ร่างกายเราทำอะไรกับยา" เช่นเราให้สัตว์ทดลองกินยาลงไปเราก็ศึกษาดูว่ายามันถูกดูดซึมเข้ากระแสเลือดใช้เวลาประมาณเท่าใด ยาสามารถแพร่กระจายไปทั่วร่างกายใช้เวลาประมาณเท่าไหร่ ยาถูกmetabolism และขับออกอย่างไร
- pharmacodynamics คือ "ยาทำอะไรกับร่างกายของเรา" อันนี้ถือได้ว่าเป็นการดูเลยครับว่ายาแก้ปวดของเรามันแก้ปวดจริงๆมั้ย และมีผลข้างเคียงอย่างไร
สมมติจากร้อยกว่าโมเลกุลได้ผ่านเข้ารอบมาถึงรอบนี้ อาจเหลือโมเลกุลที่ถูกตัดจนเหลือเพียงแค่ไม่กี่ตัวสมมติว่าเหลือ 5 ตัวนะครับ จากโมเลกุลเป็นหมื่นมาสู่ขั้นนี้ได้
ใช้ระยะเวลาเกือบ 10 ปี ใช่เเล้วครับทุกท่านอาจไม่ผิดครับ ใช้เวลาเกือบ 10 ปี แน่นอนว่าสมมติผมจบ ป.เอก ออกมาทำวิจัยยาตอนอายุ30ปี กว่าจะมาขั้นนี้ได้ผมก็คงอายุเกือบ 40 ปีแล้ว
ถ้าผมโสดตั้งแต่ตอน30ผมคงมองว่ากว่าจะได้ยาตัวนึงผมคงจะขึ้นคานทองคำแท้แน่นอน 5555 ต้องรีบโฆษณาตัวเองว่าโสดโปรดจีบ

55555 กลับมาสู่เรื่องของเราต่อครับ
เมื่อผ่านการศึกษาทั้งในห้องแลป เครื่องมือและสัตว์ทดลองแล้ว ตอนนี้ก็ได้เวลาสำคัญแล้วครับ กับโมเลกุลยาที่เหลือเพียง 5 ตัว นั้นคือถึงเวลาที่เราจะต้องเอายาเหล่านี้ไป
ลองศึกษาในมนุษย์อย่างเราๆท่านๆแล้ว
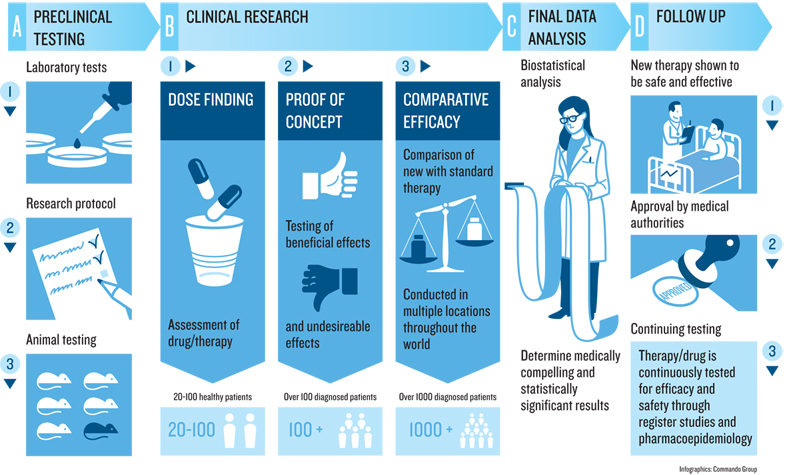 ภาพแสดงการศึกษาในขั้น Pre clinical และ Clinical trials แหล่งที่มา : http://nta.nordforsk.org
3. Clinical trials
ภาพแสดงการศึกษาในขั้น Pre clinical และ Clinical trials แหล่งที่มา : http://nta.nordforsk.org
3. Clinical trials : ขั้นตอนนี้ ถือเป็นขั้นตอนที่มีความสำคัญมาก เพราะเนื่องจากจะเป็นขั้นตอนที่ตัดสินได้เลยว่า โมเลกุลที่เราอุส่าคัดสรรเป็นอย่างดีแล้ว มีโมเลกุลใดบ้างที่จะเข้ารอบชิงชนะเลิศ สามารถออกฤทธิ์ในร่างกายคน รักษาอาการปวดได้จริง โดยที่ไม่เป็นอันตราย มีประสิทธิภาพ และมีคุณภาพจริงๆ ขั้นตอนนี้ จะเป็นขั้นตอนที่บุคลากรทางสาธารณสุขฯจะมาร่วมมือกันทั้ง นักวิจัยอย่างเรา แพทย์ เภสัช พยาบาล ที่จะเฝ้าติดตามผลการใช้ยาในคนจริงๆ โดยขั้นตอนนี้เราสามารถแบ่งออกได้เป็น 3 phase หลักๆครับคือ
- Phase 1 ศึกษาในอาสาสมัครสุขภาพดี จำนวนน้อย ประมาณร้อยคน
ขั้นนี้ศึกษาขึ้นเพื่อต้องการดูว่ายาที่เราศึกษามานั้นมีความปลอดภัยในคนจริงๆ และนอกจากจะปลอดภัยในคนแล้วอาจทำให้ทราบถึงขนาดยาที่เหมาะสม
- Phase 2 ศึกษาในอาสาสมัครที่ป่วยเป็นโรค จำนวนน้อยเช่นกัน
ขั้นตอนนี้ศึกษาขึ้นเพื่อต้องการประเมินประสิทธิภาพในโรคนั้นๆและติดตามผลข้างเคียงระยะสั้นที่อาจเกิดขึ้น
- Phase 3 ศึกษาในอาสาสมัครที่ป่วยเป็นโรค จำนวนมาก เป็นพันรายพร้อมๆกันในโรงพยาบาลหลายๆแห่ง โดยอาจจะต้องมีการทำเป็นงานวิจัยเพื่อให้ผลที่ได้นั้นมีความถูกต้อง เช่นการทำ RCT double blind หรือก็คือให้ยาจริงกับยาหลอกกับคนไข้ (คำว่ายาหลอกหรือ placebo อาจหมายถึง ตำรับยาที่ไม่มีตัวยาอยู่เลย หรือเป็นตำรับยามาตรฐานที่ใช้ในการรักษาโรคนั้นๆเช่นบอกว่าจะทำยาแก้ปวดเราก็แบ่งคนไข้เป็นสองกลุ่ม กลุ่มนึงได้ยาใหม่ที่เราคิดค้นขึ้น อีกกลุ่มได้ พาราแก้ปวด)
ขั้นตอนนี้ทำการศึกษาขึ้นเพื่อ ทำให้ทราบว่าโมเลกุลหรือยาใหม่ที่เราคิดค้นขึ้นมันมีประสิทธิภาพในการรักษามากกว่าหรือน้อยกว่าการรักษาแบบเดิม และทราบถึงผลข้างเคียงต่างๆของยาที่มากขึ้น
และแล้วในที่สุดจากโมเลกุลเป็นหมื่นเป็นพันถูกคัดเลือกผ่านมาเรื่อยๆจนถึงขั้นนี้เเล้ว หากเหลือ 5 ตัว ผมขอสมมติเป็นโมเลกุล A B C D E นะครับ มาศึกษาในคนไข้กลับพบว่า
E : ศึกษาใน phase 1 พบว่าใช้แค่ไม่กี่ dose เท่านั้นทำให้คนที่ทานเกิดผื่นแพ้อย่างรุนแรง -> E ถูกคัดออกจากการแข่งขันทันที พร้อมบันทึกเป็นตราบาปไว้เลยว่าก่อให้เกิดผื่นแพ้รุนแรง (*บันทึกไว้เพื่ออนาคตเกิดเราอยากเอามันมาพัฒนาโครงสร้างใหม่ให้ลดการเกิดผื่นแพ้ได้)
D,C,B : ศึกษาในคนไข้พบว่าก่อให้เกิดพิษต่อตับอย่างรุนแรง ทำให้คนไข้ตับวาย แน่นอนว่า -> D,C,B ถูกคัดออกจากการแข่งขัน
สุดท้าย ถ้า
A ศึกษาแล้วพบว่าไม่เกิดผลข้างเคียงรุนแรง แถมมีประสิทธิภาพการรักษาที่ดี นั้นคือข่าวดีครับ
ยินดีด้วย เราได้ยาใหม่ที่ดี สามารถแบกไป อย. เพื่อขอขึ้นทะเบียนยามาจำหน่ายในประเทศได้เเล้ว แต่!!!! เอาจริงๆถึงขึ้นทะเบียนได้ ก็ยังต้องถูกจำกัดการใช้ในโรงพยาบาลก่อนครับ เราจะเรียกว่ายาที่ออกใหม่และถูกจำกัดการใช้ในโรงพยาบาลนี้ว่า ยาติดสามเหลี่ยมครับ หรือ SMP ก็จะเข้าสู่ขั้น4
4. Regulatory approval and Post market surveillance : เป็นขั้นตอนสุดท้ายแล้วนะครับ จากผู้เข้าแข่งขันกว่าหมื่นราย เราได้คัดแล้วคัดอีกจนได้ยาขึ้นทะเบียนชนะเลิศ 1 ตัว
กว่าจะมาถึงขั้นนี้ได้ ใช้เวลา เกือบ 15-20 ปี เอาเป็นว่าย้อนกลับไปใหม่ ที่ผมบอกว่าผมจบ ป.เอก มาทำวิจัย ตอน 30 ถ้ามาถึงขั้นสุดท้ายนี้ใช้เวลาสัก 15 ปี ผมก็จะอายุ 45 คือแน่นอนว่าถ้าโสด ก็จะเป็นคานทองที่มีความบริสุทธิ์สูงมาก Purity 105% 55555

ยย กลับมาเข้าเรื่องต่อครับ
ขั้นตอนนี้คือ ยาเราจะต้องไปสิงอยู่ที่โรงพยาบาลก่อนอย่างน้อย 2 ปี หรือจนกว่าจะมีการศึกษาการใช้ในคนไข้ หมื่นราย แล้วพบว่า ไม่เกิดผลข้างเคียงที่รุนแรงถึงชีวิต ฟังดูง่ายมั้ยครับ? อาจฟังดูง่าย แต่ถ้าเราลองมองย้อนกลับไปตั้งแต่วันแรกที่เราเริ่มทำงานวิจัยยาใหม่นี้กันนะครับลองคิดเล่นๆถึง
- ระยะเวลาที่เสียไป : แน่นอนว่า มาถึงขั้นนี้ 15-20 ปี นานมากเลยครับถ้ามีลูก ลูกคงเข้าเรียนมหาวิทยาลัยแล้วครับ
- ต้นทุน cost รายจ่ายที่เสียไป : แน่นอนว่าผมบอกได้เลยว่า
จำนวนเงินที่สูญไปนั้น ไม่ต่ำกว่าหลักล้านหรือสิบล้านหรืออาจจะร้อยล้านเลยทีเดียว แน่นอนว่าคนที่จะจ่ายเงินมหาศาลขนาดนี้ได้คือใครครับ ก็จะเป็นหน่วยงาน หรือบริษัทเอกชนครับ แน่นอนว่าการจ่ายเงินระดับนี้ ย่อมมาพร้อมความคาดหวังที่สูงริ่ว
แล้วถ้ามาถึงขั้นนี้ ผลปรากฏว่าลองใช้ในโรงพยาบาลยังไม่ถึงปี ปรากฏว่ามีผลข้างเคียงรุนแรง หรือรอด SMP ได้เข้าสู่ตลาดยังไม่ทันไรเจอผลข้างเคียงรุนแรงจนต้องถอนยาออกห้ามจำหน่าย
บอกได้คำเดียวครับว่า
 แต่ถ้าไม่เกิดปัญหาอย่างว่า ก็ถือว่าโชคดีมากๆครับ เพราะจะมีเรื่องของสิทธิบัตรคุ้มครองให้ผู้คิดค้น บริษัทมีสิทธิ์ขายยานั้นเพียงรายเดียว ในราคาที่สูงริ่วเพื่อชดเชยกับที่ลงทุนไปมหาศาล ดังนั้นอย่าแปลกใจครับทำไมยาใหม่ ดีๆ ถึงราคาแพงมาก
แต่ถ้าไม่เกิดปัญหาอย่างว่า ก็ถือว่าโชคดีมากๆครับ เพราะจะมีเรื่องของสิทธิบัตรคุ้มครองให้ผู้คิดค้น บริษัทมีสิทธิ์ขายยานั้นเพียงรายเดียว ในราคาที่สูงริ่วเพื่อชดเชยกับที่ลงทุนไปมหาศาล ดังนั้นอย่าแปลกใจครับทำไมยาใหม่ ดีๆ ถึงราคาแพงมาก
ดังนั้นทุกอย่างที่ผมเล่ามาจนถึงตอนนี้ทุกท่านคงได้เห็นภาพรวมกว้างๆของการกว่าจะได้ยามาแล้วนะครับ ทุกอย่างมันกดดันนักวิจัยจริงๆครับทั้งเงิน เวลา ที่สำคัญถ้ามัน Failed จนต้องพับโครงการทุกอย่างที่ทำมาเท่ากับสูญอย่างในภาพยนตร์สั้นเราจะเสียทุกอย่างไปฟรีๆครับ
สุดท้ายผมหวังว่าเรื่องนี้จะเป็นประโยชน์ให้ท่านไม่มากก็น้อยครับขอบคุณครับ 

กว่าจะมาเป็น "ยาใหม่" ต้องผ่านอะไรมาบ้าง (ฉบับย่อ)
ผมในฐานะของนักศึกษาคณะเภสัชฯที่ตอนนี้กำลังศึกษาและสนใจงานทางด้านวิจัยและพัฒนายาอาจจะยังมีประสบการณ์น้อย แต่วันนี้ก็อยากแชร์เรื่องราวของการที่กว่าจะมาเป็นยาให้ทุกคนได้ใช้กันในปัจจุบัน นักวิจัยต้องดิ้นรนกันขนาดไหนเพื่อให้ได้มาซึ่งยาที่มีประสิทธิภาพ มีคุณภาพ และที่สำคัญมีความปลอดภัยต่อการนำไปใช้ หากผิดพลาดประการใดต้องขออภัยมา ณ ที่นี้ ด้วยนะครับ
ในตอนนี้ผมจะให้ทุกท่านสมมติตัวเองว่า เราเป็นนักวิจัยต้องการทำยาแก้ปวดขึ้นมาสักตัวหนึ่งเราจะต้องทำอย่างไรบ้าง ?
เพื่อให้เข้าใจง่ายมากขึ้นผมจะขอแบ่งช่วงระยะเวลาในการเดินทางของยาออกเป็นช่วงๆ เป็น 4 ช่วงนะครับ
1. Drug discovery : เป็นขั้นตอนแรกสุดที่ใช้เวลาค่อนข้างยาวนาน หากเราจะวิจัยทำยาแก้ปวด เราจะต้องหาโครงสร้างโมเลกุลที่มีฤทธิ์ในการแก้ปวดให้ได้ก่อน ผมจะขอเรียกว่า Lead compound นะครับ ซึ่งการที่จะให้ได้มาซึ่ง Lead compound เราสามารถทำได้โดยเช่น
- เราอาจเอาข้อมูลความรู้ที่มีการสั่งสมมาอย่างยาวนานว่าสมุนไพรใดที่สามารถแก้ปวดได้ เช่น บรรพบุรุษเราเคยใช้ต้น Willow (ไม่ใช่ Willow ในป่า payon นะครับ) ในการแก้ปวดและอักเสบได้ ดังนั้นเราก็ลองหาดูซิว่าใน Willow มันมีสารใดบ้างที่ออกฤทธิ์แก้ปวดได้บ้างเราก็สกัดออกมาจะได้สารผสม (crude extract) ซึ่งอาจมีโมเลกุลที่สามารถแก้ปวดได้หลายร้อยตัว (เว่อร์ไป 5555)
- ถ้าแอดวานซ์ขึ้นมาเราอาจต้องไปไล่ดูผลงานศึกษาวิจัยต่างๆว่าโครงสร้างใดบ้างที่ออกฤทธิ์แก้ปวดได้บ้าง เราก็รวบรวมข้อมูลมาให้มากที่สุด
ในขั้นตอนนี้จะเห็นได้ว่าการที่เราต้องหา Lead compound ที่มีฤทธิ์แก้ปวดนั้น จะทำให้เราได้โครงสร้างทางเคมีมาเป็นหมื่นเป็นพันโครงสร้าง!!!
สาเหตุที่มีเยอะขนาดนั้นเป็นเพราะว่า โมเลกุลเหล่านั้นมีโครงสร้างส่วนหนึ่งที่สามารถออกฤทธิ์แก้ปวดได้เหมือนกัน โครงสร้างของโมเลกุลเหล่านั้น เราเรียกว่า Pharmacophore ครับ
เท่ากับตอนนี้เราโครงสร้างอยู่ในมือเป็นหมื่นเป็นพันโครงสร้าง เราจะต้องคัดเลือกเพื่อหาโครงสร้างที่สามารถออกฤทธิ์ได้ดีที่สุด มีประสิทธิภาพที่สุด ปลอดภัยและเหมาะสมในการเอามาศึกษาพัฒนาต่อ ก็จะเข้าสู่ช่วงที่ 2
2. Pre clinical : ศึกษาคัดเลือกจากหลายพันโมเลกุล การคัดเลือกโดยธรรมชาติ ?
ซึ่งก็ใช้เวลาในการศึกษาที่ค่อนข้างนานเพราะเราอาจจะต้องศึกษาฤทธิ์ของแต่ละโมเลกุลๆไปเรื่อยๆเพื่อคัดเลือกให้ได้มาซึ่ง pharmacophore การศึกษาฤทธิ์ก็อาจใช้วิธีการต่างๆในห้องแลป หรือปัจจุบันสะดวกขึ้นมากก็จะใช้คอมพิวเตอร์ในการทำนายการออกฤทธิ์ ซึ่งโปรแกรมที่ใช้เช่น Autodock เป็นต้น ก็จะทำให้การคัดเลือกโมเลกุลสามารถทำได้ง่ายมากยิ่งขึ้น แต่การใช้คอมพิวเตอร์ในการทำนายการออกฤทธิ์ก็ยังไม่สามารถตอบคำถามได้ 100 % นะครับว่าโมเลกุลของเรามันดีจริง อย่างไรก็ต้องทำการศึกษาต่อในแลปอยู่ดี แต่การใช้คอมฯนั้นก็จะสามารถช่วยตัดคัดกรองโมเลกุลอื่นๆได้เยอะมากเลยทีเดียว ทำให้จากการที่เราต้องมานั่งสังเคราะห์โมเลกุลเพื่อเอาไปศึกษาผลในแลปเป็นหมื่นโมเลกุล(เหนื่อยตายก่อน)ก็อาจถูกตัดทอนเหลือไม่ถึงพันโมเลกุล
การทดลองในขั้น Pre clinical นี้จะต้องทำการศึกษาหลายขั้น ผมขอแบ่งง่ายๆเป็น
ภาพแสดง in vitro study, in vivo study แหล่งที่มา : http://invivotransfection.com
- in vitro study คือการทำการศึกษาประสิทธิภาพในการออกฤทธิ์ในเครื่องมือเครื่องแก้ว เช่นการทดลอง dpph assay ขั้นนี้จะไม่ใช้สัตว์ทดลองครับ
- in situ study คือการทำการศึกษาประสิทธิภาพในเฉพาะอวัยวะนั้นๆ เช่นการศึกษาการยึดเกาะของยาบริเวณลำไส้ หรือการทดลองการคงอยู่ของยาในดวงตากระต่าย ขั้นนี้มีการใช้สัตว์ทดลองครับ หรือบางทีอาจใช้แค่บางส่วนครับ
- in vivo study คือการทำการศึกษาในสัตว์ทดลองเลยครับ แน่นอนว่าหลังการทดลองกับสัตว์ทดลองแล้วเราต้องฆ่าสัตว์ทดลองด้วยวิธีการที่ไม่ทำให้เขาเจ็บปวดครับ T^T
ผลการศึกษาทั้งหมดจะทำให้เราทราบได้อย่างคร่าวๆว่า โมเลกุลที่เรามีอยู่เป็นร้อยนั้น แต่ละตัวมีประสิทธิภาพในการออกฤทธิ์อย่างไร มีความเป็นพิษต่อสัตว์ทดลองมั้ย (Toxicity) ถ้ามีก็ตัดทิ้ง ทำให้เรารู้ข้อมูลทางด้าน pharmacokinetics, pharmacodynamics อย่างคร่าวๆ เพื่อช่วยให้เราคัดเลือกโมเลกุลที่จะผ่านเข้ารอบต่อไปได้ง่ายขึ้นครับ
- pharmacokinetics คือ "ร่างกายเราทำอะไรกับยา" เช่นเราให้สัตว์ทดลองกินยาลงไปเราก็ศึกษาดูว่ายามันถูกดูดซึมเข้ากระแสเลือดใช้เวลาประมาณเท่าใด ยาสามารถแพร่กระจายไปทั่วร่างกายใช้เวลาประมาณเท่าไหร่ ยาถูกmetabolism และขับออกอย่างไร
- pharmacodynamics คือ "ยาทำอะไรกับร่างกายของเรา" อันนี้ถือได้ว่าเป็นการดูเลยครับว่ายาแก้ปวดของเรามันแก้ปวดจริงๆมั้ย และมีผลข้างเคียงอย่างไร
สมมติจากร้อยกว่าโมเลกุลได้ผ่านเข้ารอบมาถึงรอบนี้ อาจเหลือโมเลกุลที่ถูกตัดจนเหลือเพียงแค่ไม่กี่ตัวสมมติว่าเหลือ 5 ตัวนะครับ จากโมเลกุลเป็นหมื่นมาสู่ขั้นนี้ได้ ใช้ระยะเวลาเกือบ 10 ปี ใช่เเล้วครับทุกท่านอาจไม่ผิดครับ ใช้เวลาเกือบ 10 ปี แน่นอนว่าสมมติผมจบ ป.เอก ออกมาทำวิจัยยาตอนอายุ30ปี กว่าจะมาขั้นนี้ได้ผมก็คงอายุเกือบ 40 ปีแล้ว ถ้าผมโสดตั้งแต่ตอน30ผมคงมองว่ากว่าจะได้ยาตัวนึงผมคงจะขึ้นคานทองคำแท้แน่นอน 5555 ต้องรีบโฆษณาตัวเองว่าโสดโปรดจีบ
เมื่อผ่านการศึกษาทั้งในห้องแลป เครื่องมือและสัตว์ทดลองแล้ว ตอนนี้ก็ได้เวลาสำคัญแล้วครับ กับโมเลกุลยาที่เหลือเพียง 5 ตัว นั้นคือถึงเวลาที่เราจะต้องเอายาเหล่านี้ไปลองศึกษาในมนุษย์อย่างเราๆท่านๆแล้ว
ภาพแสดงการศึกษาในขั้น Pre clinical และ Clinical trials แหล่งที่มา : http://nta.nordforsk.org
3. Clinical trials : ขั้นตอนนี้ ถือเป็นขั้นตอนที่มีความสำคัญมาก เพราะเนื่องจากจะเป็นขั้นตอนที่ตัดสินได้เลยว่า โมเลกุลที่เราอุส่าคัดสรรเป็นอย่างดีแล้ว มีโมเลกุลใดบ้างที่จะเข้ารอบชิงชนะเลิศ สามารถออกฤทธิ์ในร่างกายคน รักษาอาการปวดได้จริง โดยที่ไม่เป็นอันตราย มีประสิทธิภาพ และมีคุณภาพจริงๆ ขั้นตอนนี้ จะเป็นขั้นตอนที่บุคลากรทางสาธารณสุขฯจะมาร่วมมือกันทั้ง นักวิจัยอย่างเรา แพทย์ เภสัช พยาบาล ที่จะเฝ้าติดตามผลการใช้ยาในคนจริงๆ โดยขั้นตอนนี้เราสามารถแบ่งออกได้เป็น 3 phase หลักๆครับคือ
- Phase 1 ศึกษาในอาสาสมัครสุขภาพดี จำนวนน้อย ประมาณร้อยคน ขั้นนี้ศึกษาขึ้นเพื่อต้องการดูว่ายาที่เราศึกษามานั้นมีความปลอดภัยในคนจริงๆ และนอกจากจะปลอดภัยในคนแล้วอาจทำให้ทราบถึงขนาดยาที่เหมาะสม
- Phase 2 ศึกษาในอาสาสมัครที่ป่วยเป็นโรค จำนวนน้อยเช่นกัน ขั้นตอนนี้ศึกษาขึ้นเพื่อต้องการประเมินประสิทธิภาพในโรคนั้นๆและติดตามผลข้างเคียงระยะสั้นที่อาจเกิดขึ้น
- Phase 3 ศึกษาในอาสาสมัครที่ป่วยเป็นโรค จำนวนมาก เป็นพันรายพร้อมๆกันในโรงพยาบาลหลายๆแห่ง โดยอาจจะต้องมีการทำเป็นงานวิจัยเพื่อให้ผลที่ได้นั้นมีความถูกต้อง เช่นการทำ RCT double blind หรือก็คือให้ยาจริงกับยาหลอกกับคนไข้ (คำว่ายาหลอกหรือ placebo อาจหมายถึง ตำรับยาที่ไม่มีตัวยาอยู่เลย หรือเป็นตำรับยามาตรฐานที่ใช้ในการรักษาโรคนั้นๆเช่นบอกว่าจะทำยาแก้ปวดเราก็แบ่งคนไข้เป็นสองกลุ่ม กลุ่มนึงได้ยาใหม่ที่เราคิดค้นขึ้น อีกกลุ่มได้ พาราแก้ปวด) ขั้นตอนนี้ทำการศึกษาขึ้นเพื่อ ทำให้ทราบว่าโมเลกุลหรือยาใหม่ที่เราคิดค้นขึ้นมันมีประสิทธิภาพในการรักษามากกว่าหรือน้อยกว่าการรักษาแบบเดิม และทราบถึงผลข้างเคียงต่างๆของยาที่มากขึ้น
และแล้วในที่สุดจากโมเลกุลเป็นหมื่นเป็นพันถูกคัดเลือกผ่านมาเรื่อยๆจนถึงขั้นนี้เเล้ว หากเหลือ 5 ตัว ผมขอสมมติเป็นโมเลกุล A B C D E นะครับ มาศึกษาในคนไข้กลับพบว่า
E : ศึกษาใน phase 1 พบว่าใช้แค่ไม่กี่ dose เท่านั้นทำให้คนที่ทานเกิดผื่นแพ้อย่างรุนแรง -> E ถูกคัดออกจากการแข่งขันทันที พร้อมบันทึกเป็นตราบาปไว้เลยว่าก่อให้เกิดผื่นแพ้รุนแรง (*บันทึกไว้เพื่ออนาคตเกิดเราอยากเอามันมาพัฒนาโครงสร้างใหม่ให้ลดการเกิดผื่นแพ้ได้)
D,C,B : ศึกษาในคนไข้พบว่าก่อให้เกิดพิษต่อตับอย่างรุนแรง ทำให้คนไข้ตับวาย แน่นอนว่า -> D,C,B ถูกคัดออกจากการแข่งขัน
สุดท้าย ถ้า A ศึกษาแล้วพบว่าไม่เกิดผลข้างเคียงรุนแรง แถมมีประสิทธิภาพการรักษาที่ดี นั้นคือข่าวดีครับ
ยินดีด้วย เราได้ยาใหม่ที่ดี สามารถแบกไป อย. เพื่อขอขึ้นทะเบียนยามาจำหน่ายในประเทศได้เเล้ว แต่!!!! เอาจริงๆถึงขึ้นทะเบียนได้ ก็ยังต้องถูกจำกัดการใช้ในโรงพยาบาลก่อนครับ เราจะเรียกว่ายาที่ออกใหม่และถูกจำกัดการใช้ในโรงพยาบาลนี้ว่า ยาติดสามเหลี่ยมครับ หรือ SMP ก็จะเข้าสู่ขั้น4
4. Regulatory approval and Post market surveillance : เป็นขั้นตอนสุดท้ายแล้วนะครับ จากผู้เข้าแข่งขันกว่าหมื่นราย เราได้คัดแล้วคัดอีกจนได้ยาขึ้นทะเบียนชนะเลิศ 1 ตัว
กว่าจะมาถึงขั้นนี้ได้ ใช้เวลา เกือบ 15-20 ปี เอาเป็นว่าย้อนกลับไปใหม่ ที่ผมบอกว่าผมจบ ป.เอก มาทำวิจัย ตอน 30 ถ้ามาถึงขั้นสุดท้ายนี้ใช้เวลาสัก 15 ปี ผมก็จะอายุ 45 คือแน่นอนว่าถ้าโสด ก็จะเป็นคานทองที่มีความบริสุทธิ์สูงมาก Purity 105% 55555
ขั้นตอนนี้คือ ยาเราจะต้องไปสิงอยู่ที่โรงพยาบาลก่อนอย่างน้อย 2 ปี หรือจนกว่าจะมีการศึกษาการใช้ในคนไข้ หมื่นราย แล้วพบว่า ไม่เกิดผลข้างเคียงที่รุนแรงถึงชีวิต ฟังดูง่ายมั้ยครับ? อาจฟังดูง่าย แต่ถ้าเราลองมองย้อนกลับไปตั้งแต่วันแรกที่เราเริ่มทำงานวิจัยยาใหม่นี้กันนะครับลองคิดเล่นๆถึง
- ระยะเวลาที่เสียไป : แน่นอนว่า มาถึงขั้นนี้ 15-20 ปี นานมากเลยครับถ้ามีลูก ลูกคงเข้าเรียนมหาวิทยาลัยแล้วครับ
- ต้นทุน cost รายจ่ายที่เสียไป : แน่นอนว่าผมบอกได้เลยว่า จำนวนเงินที่สูญไปนั้น ไม่ต่ำกว่าหลักล้านหรือสิบล้านหรืออาจจะร้อยล้านเลยทีเดียว แน่นอนว่าคนที่จะจ่ายเงินมหาศาลขนาดนี้ได้คือใครครับ ก็จะเป็นหน่วยงาน หรือบริษัทเอกชนครับ แน่นอนว่าการจ่ายเงินระดับนี้ ย่อมมาพร้อมความคาดหวังที่สูงริ่ว
แล้วถ้ามาถึงขั้นนี้ ผลปรากฏว่าลองใช้ในโรงพยาบาลยังไม่ถึงปี ปรากฏว่ามีผลข้างเคียงรุนแรง หรือรอด SMP ได้เข้าสู่ตลาดยังไม่ทันไรเจอผลข้างเคียงรุนแรงจนต้องถอนยาออกห้ามจำหน่าย
บอกได้คำเดียวครับว่า
ดังนั้นทุกอย่างที่ผมเล่ามาจนถึงตอนนี้ทุกท่านคงได้เห็นภาพรวมกว้างๆของการกว่าจะได้ยามาแล้วนะครับ ทุกอย่างมันกดดันนักวิจัยจริงๆครับทั้งเงิน เวลา ที่สำคัญถ้ามัน Failed จนต้องพับโครงการทุกอย่างที่ทำมาเท่ากับสูญอย่างในภาพยนตร์สั้นเราจะเสียทุกอย่างไปฟรีๆครับ
สุดท้ายผมหวังว่าเรื่องนี้จะเป็นประโยชน์ให้ท่านไม่มากก็น้อยครับขอบคุณครับ